前言
由于B群链球菌(Group B Streptococcus,
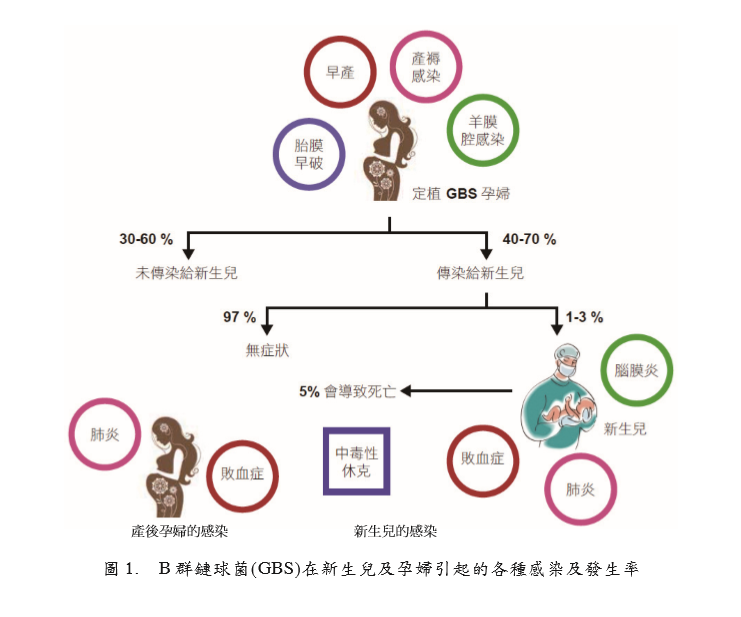
Streptococcus agalactiae, GBS,乙型链球 菌)可引起新生儿的肺炎(pneumonia)、脑膜
炎(meningitis)和败血症(sepsis)以及产妇败血
症及肺炎(图1)[1, 2],美国疾病控制与预防 中心(Centers for Disease Control and Prevention, CDC)建议怀孕35~37周之妇女需进行阴道
及/或肛门拭子的 GBS 检测,以期在分娩前
施与抗生素。此措施成功地降低新生儿GBS 感染率达75%以上,也使致死率由1970年的 50%大幅下降至1990年的5% [3]。在台湾, 卫生福利部国民健康署也为了提升产前GBS 检查的普及率,于2014年 4 月起将 GBS 检
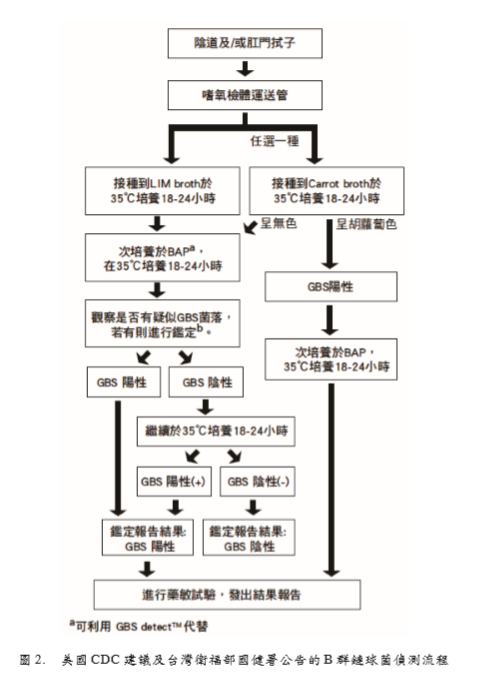
测费纳入健保给付[4]根据美国CDC建议以及卫福部国健署委 托台湾医事检验学会拟定的侦测B 群链球菌 标准作业流程[3, 5](图2),建议以无菌棉拭 自阴道及/或直肠采检后插入嗜氧检体运送管 (aerobic transport medium),送到检验室后,先划种血琼脂平板(BAP),再将棉拭插入Lim broth(纯增菌用)或carrot broth(增菌与鉴 别用),在35℃一般恒温箱培养18~24小时 后,若 BAP 上有疑似 GBS 的 -溶血型菌落
则需进行CAMP (Christie, Atkins, and MunchPetersen)、hippurate(马尿酸)水解或链球 菌分群试验加以确认,如无发现疑似菌落, 则再将 Lim broth 增菌液再次移种一血琼脂 平板,所有培养基均继续培养18~24小时, 再发出最终报告。若接种carrot broth,则检 视其是否显色,若呈胡萝卜色即可报告为GBS 阳性,若呈阴性,则再接种 GBS DetectTM (Hardy公司,美国),若有 -溶血型菌落, 则需如同Lim broth所移种BAP上的疑似菌 落进行确认试验,如无发现疑似菌落,则所 有培养基均继续培养18~24小时,再发出最
终报告。
虽然美国CDC及卫福部国健署的建议流 程可将 GBS 的检验标准化,但所用的 Lim broth增菌培养基方法需经过多次移种培养确
认,将会延迟报告3~4天[6],而carrot broth 的接种需加一条促进产色纸条[7],以及所建 议移种的 GBS DetectTM 伪阳性高达58% (62/107) [8],造成检验人员的不便以及鉴定
人力与物力的浪费。由于使用嗜氧检体运送 管运送检体不能立即增菌,并可能让产道或 肠道栖息菌增生进而干扰GBS的检出。有鉴
于上述美国CDC及卫福部国健署建议方法的 诸多缺点,启新生物科技有限公司(新北市, 台湾)遂设计孕妇产前检查B 群链球菌的简 易高效快检套组,其系由运送装置 CMPTM GBS
TransCultSwab(GBS 的运送增菌培养 管)[9]结合 / GBS detection agar(侦测琼 脂)[10] / GBS
carrot agar(GBS 胡萝卜琼脂)[11]分隔平板(Bi-plate)而组成,此套组以 简易操作、高检出率(分离率)及可缩短报 告时间与减少检验人员操作人力做为要求。 本研究将评估 GBS TransCultSwab 结合 / GBS detection agar /
GBS carrot agar分隔平 板的移种以确认其在临床实际应用的有效性。
材料与方法 :
GBS检验套组的组成 GBS 简易高效快检套组的组成包括 CMPTM GBS TransCultSwab[9]与 / GBS detection
agar[10] / GBS carrot agar[11]分隔平板,每一个孕妇使用一支GBS
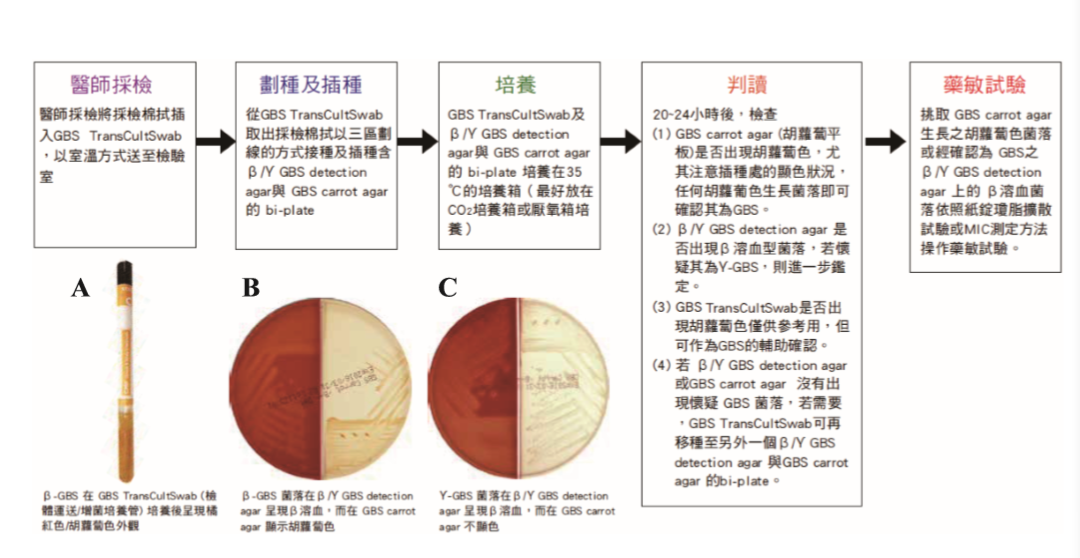
TransCultSwab 及一个分隔平板,分别介绍如下: GBS TransCultSwab(图3A):GBS TransCultSwab(专利证书I627277号)是一 种结合采检、运送、增菌与GBS假设性鉴定 四种功能的装置,包装中含有一支塑料管,
内含可让 GBS 增菌与实时抑制其它产道/直 肠栖息菌生长的培养基配方,以及使GBS的 -溶血株生长后显色的成份,以半固体的方式 配制以利运送;装置中另附一支无菌棉拭作
为采集产道及/或直肠分泌物检体之用。医师 采检时将棉拭取出插入产道及(或)直肠约 2~3公分处旋转两圈采取足量分泌物后插至 含增菌培养基的塑料管中,在室温或35℃恒
温箱暂时保存,然后在最短的时间内送至微 生物检验室,检验室收到此运送装置,登记 相关数据后,置于35℃的一般或 CO2 恒温 箱,培养5~24小时后可在任何时间内取出棉 拭移种至套组的分隔平板。 / GBS detection agar / GBS carrot agar 分隔平板:分隔平板中的 GBS carrot agar(专利证书I627277号)系针对GBS 溶血型菌株的侦测而设计的固体培养基,GBS carrot agar 含有特殊显色基元可让 -溶血型 GBS 的生长菌落呈胡萝卜色(图3B 的右半 边,呈米白色), / GBS detection agar(专
利证书I561634号)系针对GBS -溶血型菌 株的侦测而设计。含有绵羊血与特殊的溶血
加强液,可让 -溶血型菌落转变成 -溶血型 (图3C的左半边,呈红色),而其接种方法 (图3 之操作流程)为取出 GBS Trans CultSwab 的棉拭划种分隔平板的两边各约 1/3,然后利用接种环操作三区划线技术,最
后在分隔平板的第一区培养基各插种5~7次, 接着放在35℃的一般或CO2恒温箱培养20~48 小时。由于其它少数菌在 / GBS detection agar 的生长菌落亦同样地呈 -溶血,因此,
培养后任何怀疑的生长菌落需再进行适当的鉴定试验(如CAMP试验、马尿酸试验或血 清分群试验)加以确认。
以临床检体实际评估GBS简易高效快检套组 从 2016年 4 月 1 日至2017年 3 月 31日 止,新北市某医事检验所以CMPTM GBSTrans CultSwab 采检744个产前 GBS 检查检体, 采集依产科门诊的作业习惯暂时保存在室温 或 35℃的一般或5 % CO 2 恒温箱,再以常温 方式运送至微生物检验室,放入35℃的一般
或 5% CO2 恒温箱培养5~24小时。若中午前 收到检体,则培养后在下班前一小时移种至
含 / GBS detection agar / GBS carrot agar 的分隔平板;若在中午后收到检体,则培养
至次日早上移种。移种的方式如上述的分隔 平板使用说明。接着,将GBS TransCultSwab 与分隔平板培养置入35℃的一般或CO2 恒温 箱培养20~48 小时,然后进行判读,若在 GBS carrot agar的生长菌落呈橘~红色,且 在 / GBS detection agar呈现 -溶血现象即 可鉴定为GBS(图3B及表1),又若在GBS carrot agar的生长菌落不呈色,但在 / GBS detection
agar 呈现 -溶血现象(图3C 及表 1),则必须操作必要的鉴定试验(如CAMP 试验、马尿酸试验或血清分群试验)加以确
认。
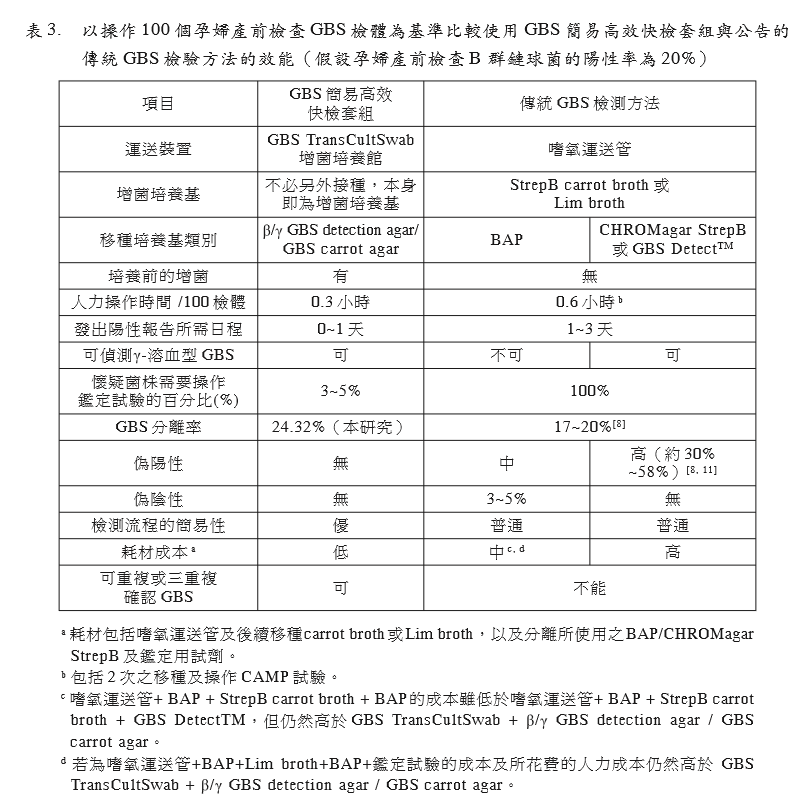
GBS 简易、高效及快检技术所用套组与传统 检验方法的成本与效能比较 以操作100个产前GBS检查检体为例, 假设 GBS 阳性率为20%,将所评估的 GBS 简易高效快检套组与当前传统检验方法进行 成本、操作方式、效能等比较。
结果 以临床检体实际评估GBS简易高效快检套组 利用 GBS 简易高效快检套组(结合 CMPTM GBS TransCultSwab与 / GBS detection
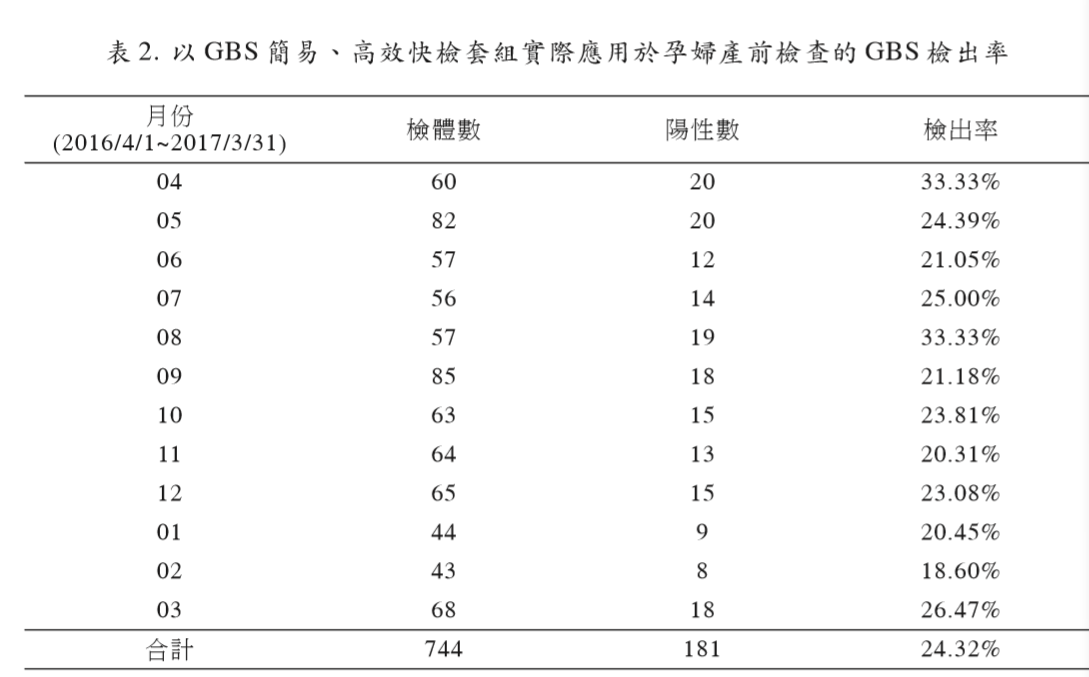
agar / GBS carrot agar 分隔平板)在12个月 间共评估744 个临床产前检查检体,结果发 现孕妇的 GBS 检出率(阳性率)为 24.32%
(181/744),月的检出率约介于18.60%~33.33%。 (表2)
GBS 简易、高效及快检套组与公告的传统检 验方法、成本与效能比较 以操作100个产前 GBS 检查检体为例,假设GBS阳性率为20%,将GBS简易、高效 快检套组与公告的传统的 GBS 检测方法进行 成本与效能比较,传统检测方法为利用嗜氧 运送管采检及运送,送至检验室后接种血平 板或显色平板(CHROMagar StrepB)以及Lim broth或carrot broth,培养后进行判读,结果 显示 GBS 简易高效快检套组在操作时间、检
出率、报告时效、成本以及简易性等项目皆 优于公告的传统GBS检测方法。(表3)。
讨论
GBS 的孕妇带原者约为15~30%[12-17],
医师对带原者常用的预防用药为 penicillin [3],其施用时机为分娩前4 小时,但若孕妇 对其过敏,则检验室需提供其它适当药物的 药敏型式。又如果发生早产,羊水提早破裂, 胎儿很可能因此受到感染。因此在孕妇产前 GBS检查的正确性与快速性对预防性抗生素 的应用将具有重要性。 传统孕妇产前GBS检验方法为采检后送
至检验室立即接种BAP或其它选择区分性显 色琼脂(如CHROMagar
StrepB),然而两 者 GBS 检出率不高,仅为7.5%[18]以及 9.7~11.8%[19],且BAP 与显色平板生长菌落 对 GBS 均不具有特异性,前者为滋养培养 基,革兰氏阳性及阴性菌都可以生长,而后 者有许多其它菌如Streptococcus pneumoniae Streptococcus pyogenes (GAS)、Group G Streptococcus (GGS)、Staphylococcus
aureus、 S. epidermidis与Stenotrophomonas
maltophilia 的生长菌落也呈现与GBS同样的紫色菌落形态,而无法彼此区分,CHROMagar StrepB 显色琼脂的特异性仅达70% (24/40)[11],此
发现与CHROMagar StrepB显色琼脂的使用 说明一致[20]。因此,在实际应用时,任何紫
色菌落在CHROMagar StrepB的出现还需进 行 CAMP 或 hippurate 水解等鉴定试验以确 认分离菌为GBS,此额外试验将延迟检验报
告 1 天,也更浪费人力及物力。另外,林等 [21]以 PCR DNA方法检测晚孕期阴道B 群链 球菌的定植分别发现其检出率为14.1% (288/1,472),而杨等[22]及季等[23]应用实时萤 光定量PCR技术指出GBS的阳性率为13.5% (85/600)与 4.17% (377/9,073)。分子诊断技
术虽然快速获得检测结果,但检出率不高, 且萃取检体中的菌体DNA,不仅费时、成本 高、须有昂贵的设备与良好的实验室环境以
及胜任的操作人员,且无法实时获得进行药 敏试验所需的GBS生长菌落,美国的疾病管 制署(CDC)[3]并不建议使用分子检测方法直 接从孕妇产前检体侦测GBS。 本研究指出GBS简易、高效快检套组证 实 CMPTM GBS TransCultSwab具有采检/运送/增菌及假设性鉴定 GBS 的效能,检验人
员的使用将不需再移种增菌培养基(Lim broth 或carrot
broth),也不需如同美国Hardy生产 的carrot
broth需额外插入加强显色纸条,因 此 GBS TransCultSwab的操作堪称简易、方 便与亲民(user friendly)。另外,GBS Trans CultSwab移种的分隔平板中GBS carrot agar 侦测 -溶血型GBS的特异性高达100%[11], 因此,任何橘~红色的生长菌落可借着显色特征快速检出GBS。GBS除了 -溶血型外, 尚有3~5%属于非( )溶血型[3],此可藉者分 隔平板的 / GBS detection agar快速侦测, 因此,检测套组对GBS的侦测是全面性的, 虽然美国Hardy Diagnostics已研发可用于侦 测 溶血型GBS的区分性培养基-GBS DetectTM (平板培养基),发现 溶血型 GBS 从孕妇 检体的检出率为3.9% (24/619),但因其伪阳 性高达58% (62/107)[8],将导致检验人力的浪费及伪阳性的产生,综合以上及本研究之
临床744件检体测试结果,使用 GBS Trans CultSwab搭配 / GBS detection agar / GBS carrot agar 分隔平板的移种,对GBS侦测率 (检出率)高达24.32%。(表2) 过去研究曾指出Enterococcus spp.(肠 球菌)的菌量高于 -溶血型GBS十倍时会干 扰(掩盖或抑制) -GBS在 GBS carrot agar [11]和GBS TransCultSwab的显色能力[24-26]。 推测Enterococcus spp.干扰 -GBS的原因可 能为其等同属一个菌科,生长条件相同,且
在增菌培养基的生长速度相近之故,但在相 等菌量存在时则不影响显色。目前尚无法从 配方的改变加以改善,但运送管增菌培养5 小时后,搭配 / GBS detection agar / GBS carrot agar的三区划线法移种,将可隔离GBS 与 Enterococcus spp.,而避免后者的干扰 [25], -GBS虽然在carrot
agar不显色,但可 在 / GBS detection agar产生 -溶血型菌落, 只要进行必要的 CAMP、马尿酸(hippurate) 水解或链球菌血清分群试验将可立即加以区 分[10]。
孕妇产前检查GBS分离率受到各种因素 影响[12],包括(i) 医师或护理师的采检技术: 此因素影响GBS分离率最大,如果仅采集产
道,应该将棉拭深入产道内2 公分,慢慢旋 转 2 圈已得到最大量的分泌物为原则;如果
用同一支棉拭采检直肠部位检体,也是操作 同样的采检技术。有些医师欲分别得到产道 与直肠的检体,则共取2 支无菌棉拭采检。 (ii) 特殊增菌与分离培养基的使用:GBS 的 棉拭检体不能直接接种平板培养基,必须先
经过增菌,才能移种或操作real-time PCR。 增菌肉汤培养基包括carrot
broth, Lim broth, Trans-Vag broth 以及本研究所建议的 GBS
TransCultSwab,分离培养基则包括CHROMagar StrepB、BAP、CNA、PEA、GBS DetectTM以 及本研究所建议含 / GBS detection agar/
GBSCarrot agar的bi-plate,其中GBS
DetectTM、 bi-plate 与 CHROMagar
StrepB 均能测出 GBS,但因两者伪阳性高,因此均需要挑取 GBS怀疑菌落进一步操作确认试验(如CAMP 试验)。(iii) GBS检测的操作技术以及检验 人员的训练与经验:如果直接将棉拭检体接 种 BAP 等分离培养基或操作 PCR 等分生技 术,GBS分离率仅约7~10%左右;如果仅用 GBS TransCultSwab 的培养结果,在医师正
确采检技术及检验人员对判读有6 个月以上 经验的条件下,GBS分离率为18.63% (30/161) [9]以及18.28%[21],如果没有足够的判读经
验,分离率约为11.03%[21],因此,GBSTrans CultSwab 应该配合 / GBS detection agar/ GBS Carrot agar的 bi-plate的移种才能够达 到本研究所显示的高GBS分离率(24.32%)。 (iv) / GBS detection agar/ GBS
Carrot agar 的bi-plate接种技术:由于是分隔培养基,因 此选用三区划线技术,移种的第一区约占表
面积的1/3,然后将接种环灭菌冷却后再涂画 第二区,同样地,再次将灭菌环灭菌后再涂 画第三区,最后在第一区插种5 次,以便获 得无氧环境,更利于 -GBS 在 bi-plate 分别 产生橘-红色[11]及产生 -溶血环。(v) 棉拭检 体需有足够的增菌时间:无论在carrot broth, Lim broth, Trans-Vag broth 以及GBS
Trans CultSwab均需要培养在35~37℃的CO2 培养
箱,肉汤培养基须培养20~24小时,而GBS TransCultSwab则培养5~24小时,才能移种 至CHROMagar StrepB、BAP、CNA、PEA、 GBS DetectTM 之一的分离培养基。以及(vi) 延长培养时间及再次移种:GBS 检测的棉拭 检体经过增菌、移种及培养后如果没有显示 生长,增菌培养基最好延长培养一天,然后 再进行平板培养基的移种及培养后的观察。
总之,除了提高GBS的检出率、有能力 侦测 -溶血型 GBS 以及避免 Enterococcus spp.的干扰外,本研究亦发现此套组的分隔平板在培养隔日即可鉴定出GBS,其阳性生 长菌落可随即用于操作药敏试验,如此,将 可缩短至少一天的报告时间,并且GBS
Trans CultSwab 运送管与 GBS carrot agar 上的显 色及在 / GBS detection agar呈现的 -溶血 特征将可做为三重复确认(triple-check) GBS 的存在,由于检验人员仅需移种一次,且花 费时间仅约15秒,对检验人员堪称方便,操
作人员仅需稍微训练即能进行检验工作,因 此,对临床检验室而言,GBS TransCultSwab 结合 / GBS detection agar / GBS carrot agar 的移种将具备简易、快速及高通量(highthroughput)检测的优点,值得临床检验室加 以应用,以便将阳性检验结果实时提供医师 做为预防新生儿与孕妇感染的参考。
参考文献
1. Schleifer A. Group B streptococcus. Lancet 1999; 353: 51-6. 2. Spellerberg
B, Brandt C. Streptococcus. In Jorgensen JH, Pfaller MA, Carroll KC, Funke G,
Landry ML, Richter SS, Warnock DW (eds). Manual of Clinical Microbiology. 11th
ed., 2015:383-402. ASM press, Washington DC, USA. 3. Verani JR, McGee L, Schrag
SJ. Prevention of perinatal group B streptococcal disease revised guidelines
from CDC, 2010. MMWR Recomm Rep 2010; 59:1-32. 4. 卫生福利部国民健康署。孕妇乙型链球菌筛检补助
服务方案。2012。卫生福利部国民健康署,台湾。 5. 台湾医事检验学会。乙型链球菌(GroupB Streptococcus) 检验标准作业手册。2014。台湾医事检验学会,台
湾。 6. Elsayed S, Gregson D, Church D. Comparison of direct
selective versus nonselective agar media plus LIM broth enrichment for
determination of Group B Streptococcus colonization status in pregnant women.
Arch Pathol Lab Med 2003; 127:718-20. 7. Hardy diagnostics
https://catalog.hardydiagnostics.com/ cp_prod/Content/hugo/
StrepBCarrotBrothKit.html 8. Clasen R, Cuna V, Dolan S et al. Evaluation of GBS
DetectTM: a new medium for the detection of non-hemolytic group B strep in
subcultures of carrot brothTM and Lim broth. results of a multi-center trial.
http://www. hardydiagnostics.com/pdf/sc_posters/gbs_detect_poster_c135.pdf 9. 邱彦昕,黄玉君,洪晟峯,陈诗婷,沈慧珊,蔡岳
廷,蔡文城。快速筛检B 群链球菌之简易创新设计CMPTM GBS
TranSwab。检验及品保杂志 2013; 2:49-59 10. 蔡文城、叶卜硕、蔡伟勋、洪晟峯、王彦博、蔡岳
廷、吕旭峯。CMPTM ß/ GBS Detection Agar: 一种 侦测B群链球菌 溶血型菌株的创新培养基。检验及 品保杂志2015; 4:16-22。 11. 郑仕雯、陈柔、沈慧珊、欧宇祥、蔡文城。GBSCarrot Agar鉴别B群链球菌的效能。检验及品保杂志2014; 3:85-95。 12. 庄立暐,邱彦昕,杨荣胜,陈诗婷,沈慧珊,蔡岳 廷,蔡文城。Group B
Streptococcus在临床各类检体 的分离率及药敏型式。检验及品保杂志 2013; 2:60-9。 13. 苏勋璧,谢保群,吕衍孟,吴昆哲,许权霖。台湾 地区周产期B群链球菌感染评估。疫情报导2005; 24: 336-48. 14. Schrag SJ, Zywicki S, Farley MM, et al. Group
B streptococcal disease in the era of intrapartum antibiotic prophylaxis. N
Engl J Med 2000; 342:15-20. 15. Ronald SG, Stephanie S, Anne S. Perinatal
infections due to group B streptococci. Obstet Gynecol 2004; 104: 1062-76. 16. 黄于宸,赖雅惠,黄翊娟,叶美杏,陈启芳,林建
佐,周俪伃,谢月贞。提升 B 群链球菌检出率之经 验分享。2015。台湾医事检验学会104年度会员(代 表)大会暨学术发表会,台北。 17. 郭安静,吴竹兰,吴雪颖等。GBS专用增菌液或GBS 选择性培养皿对孕妇乙型链球菌筛检阳性率的影响。 2016:89。台湾医事检验学会105年度会员(代表) 大会暨学术发表会,台北。 18. 蔡文城、蔡伟勋、吕旭峯、陈诗涵、吴佩真、韩之 詅、王彦博、李秀霞。CMPTM
GBS检体运送管配合 GBS carrot agar 的移种可提升产前检查B 群链球菌 的分离率及效率。检验及品保杂志2015; 4:51-7。 19. Akhlaghi F, Hamedi A, Nasab MN. Comparison of group B
streptococcal colonization in the pregnant diabetic and non-diabetic women.
Acta Medica Iranica 2009; 47:103-8. 20. CHROMagar. CHROMagarTM StrepB
instructions for use. www.chromagar.com. 21. 林新祝,吴健宁,张雪芹等。晚孕期阴道 B 族链球 菌定植与新生儿感染关系。中华围产医学杂志2016; 19:491-6.
22. 杨昆祥,王芬芳,钟泽艳。应用实时荧光定量 PCR 技术探讨 B 群链球菌与胎膜早破的关系。国际检验 医学杂志2016; 10:1387-8。 23. 季修庆,陆根生,胡平,成建,刘邺,林颖。荧光定量PCR 检测南京地区孕晚期妇女生殖道B 族链球 菌的带菌情况。检验医学2014; 29:628-30。 24. 蔡伟勋、何承蓉、洪晟峰、蔡文城。孕妇产前检查 乙型链球菌CMPTM GBS
carrot broth与 CMPTM GBS TransCultSwab 的效能评估。检验及品保杂志2016; 5:1-10。25. 黄玉霞,蔡文城。常见生殖道定植菌在CMPTM GBS 运送增菌培养管中的消长评估。检验及品保杂志2017; 6:172-7。 26. 黄玉霞,蔡文城。评估生殖道定植菌在CMPTM GBS 运送增菌培养管不同培养环境的消长。检验及品保
杂志2018; 7:111-8。